| このページの内容 |
老化の影響
老化とは何か?
| 老化に伴う構造ならびに機能の消失( 男性 ) 30 歳のデータを 100% とした場合の 75 歳において認められる機能の割合( % ) |
|
|---|---|
| 脳の重量 | 56 |
| 脳への血液供給量 | 80 |
| 休息時の心臓の血液拍出量 | 70 |
| 腎臓における糸球体の数 | 56 |
| 糸球体濾過量 | 69 |
| 血液の pH 緩衝能 | 17 |
| 味蕾の数 | 36 |
| 肺活量 | 56 |
| 握力 | 55 |
| 運動中の最大 O2 摂取量 | 40 |
| 脊髄神経における軸索の数 | 63 |
| 神経インパルスの速度 | 90 |
| 体重 | 88 |
老化によって,生理機能が漸進的に低下し,やがて機能が衰え死ぬ。
表には老化による機能の低下の割合を示す。
機能の低下は細胞内で確実に起こっている。これは細胞周期に入っていない( 増殖しない )細胞でも同じである。たとえば,
- 脳内のニューロン
- 骨格筋と心筋
- 腎臓
組織と器官は細胞からできている。細胞は生涯を通して,有糸分裂によって補給されている。たとえば,
- 血液
- 腸の上皮
すべての生物が老化するのか?
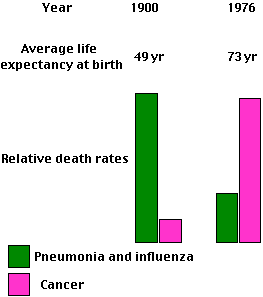
20 世紀の初めには,肺炎とインフルエンザ のような感染症の死亡率が高かった。感染症に対する効果的な対処法,すなわち抗生物質や予防接種によって平均寿命が著しく増加し,これに代わって 心疾患やガン のような器質性疾患が最も多い死亡原因に成ってきた。
答えは 否 である。 ほとんどの生物では,老化の兆候を示さない。 以下の要因のために,無作為に死亡する。
- 飢餓
- 補食
- 感染症
- 過酷な環境 ( たとえば,低温度 )
ほとんどの動物は老化の兆候を示す前に屠殺 ( 捕殺 ) されている。
事実,ヒトと人が保護しようと選択した動物 ( ペットとしてのイヌ,ネコ,オウムなど ) だけが老化する。
ヒトにおいてさえも,老化が問題となってきたのは最近数十年である。1900 年には,米国における新生児の平均寿命は 49 歳とみられていた。ほとんどの人は老化が問題となる年齢にまで達せず,死亡した。感染症が主な死因である。
約 75 年後,平均寿命は 73 歳に上昇し,死亡の主因としてガンなどの器質性疾患が感染症にとって代わってきた。
今日,平均寿命は女性では 80 歳に達し ( 男性では 74 歳 ) ,加齢人口の問題が国内の経済的ならびに社会的な問題となってきている。
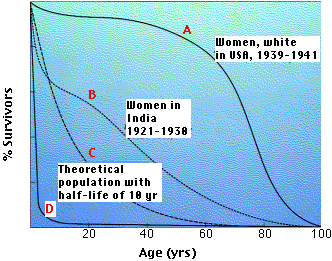
右のグラフは4つの代表的な生存曲線を示している。各年齢(横軸)における生存者の割合(縦軸)を示す。
- 曲線 A は晩年まで死亡率が低いままの生物の特徴を示す。この場合,死亡は老化の過程の終末点にますます近くなる。
- 曲線 B は飢餓や疾病などの環境の要因によって,老化の影響が明確でない ( また,新生児の死亡率が高い ) 集団の特徴を示す。
- 曲線 C はすべての年齢において死亡率が等しい生物に対する理論的な曲線である。これは老化の兆候を( あったとしても )ほとんど示さない生物(ある種の魚類),あるいは生涯を通して環境要因から死亡率が極めて高い生物 ( たとえば野生の鳥類 ) の場合に相当するだろう。
- 曲線 D は多量の子孫を生産するが,幼生の死亡率の高い,たとえばカキ ( oyster ) のような生物に特有である。
C と D の中間の生存曲線を示す生物は老化の兆候を示す機会がない。
無脊椎動物における老化
無脊椎動物は老化の過程についていくつかの重要な糸口を与えてくれる。
- 海綿動物やサンゴのような群生の無脊椎動物は老化の兆候を示さない。 78 年間生存するとされるイソギンチャクのような刺胞動物はほとんど,あるいは全く老化の兆候を示さない。 これらのすべての場合には,年数が経るにしたがい,常に古い細胞は新しい細胞によって置き換わっていると思われる。
- ロブスターも非常に長く生存するが,繁殖率や他の生理機能の低下などのような明確な兆候は認められない。しかも,ロブスターは決して成長するのを止めない。この動物が生き続ける間新しい細胞が形成され続けていると思われる。
- 培養容器の中では,ショウジョウバエ は限られた寿命をもち,死ぬ前に老化の兆候を示す。2つの要因が老化の過程と寿命に影響することが分かっている:
- カロリー制限, すなわち,半飢餓の状態の餌を与える。事実,食餌制限によって,哺乳動物を含む,検討されたすべての動物で寿命が延長することが示されている。
- 特定の遺伝子
- ショウジョウバエ,線虫ならびに酵母で寿命を延長する遺伝子が同定されている。
脊椎動物における老化
ある種の動物では,すなわち,
- 魚類
- 両生類
- 爬虫類
これらの動物は危険環境を生き延びれば,長い寿命をもつ ( ある種のカメでは 150 歳に達することが知られている ) 。
すべての事例で,これらの動物は決まった体の大きさをもたないが,生涯を通じて成長し続けている。もちろん,新たな細胞が供給され続けていると思われるが,詳細については不明である。
鳥類や哺乳動物では状況がかなり異なる。
これらの動物は決まった成体の大きさをもっており,危険環境を避けても,老化の兆候を示す。
なぜ我々は老化するのか?
1. 我々の遺伝子にプログラムされているのか?
支持する意見
- ショウジョウバエ,線虫,酵母ならびにマウスで寿命を延長する遺伝子が見つかっている。
- ヒトの家系によって,明らかに長寿命の系統がある。
反対する意見
- 生殖年齢が終了した後にだけ,有益な影響を示す遺伝子が自然淘汰をかいくぐって選択されることはない。ただし,T
- 生殖期間を延長する何らかの遺伝子,あるいは
- 長命性と同様に,若齢期にも健康を奨励する何らかの遺伝子
これらが,選抜されることはあり得るだろう。
2. 活動的な生活の必然的な結果なのか?
支持する意見
- 多くの冷血動物 ( たとえば,魚類や爬虫類 ) は老化の兆候を示さない。
- カロリー制限 によって,他の動物と同様に,鳥類や哺乳動物 ( マウスとおそらくサル ) の寿命は延長し,老化の兆候が現れるのが遅れる。これはなぜか?誰もはっきりとは分からないが,摂取カロリーを減らすことで,代謝が低下することが答えの一部であるかも知れない。代謝の大部分はミトコンドリアによる栄養素の酸化である。これらの過程によって,以下に示したような活性の高いO2-イオンを有する化合物 ( reactive oxygen species,”ROS” ) が生成される。
- 過酸化水素水 hydrogen peroxide ( H2O2 )
- 超酸化物陰イオン superoxide anion ( O2– )
カロリー制限されサルは,以下のような代謝性変化を示す:
- 低い体温
- 低いインシュリン濃度
- 副腎のステロイドホルモンである dehydroepiandrosterone sulfate ( DHEAS ) の高い濃度
これらは男性における長命性と関連が指摘されている。
Igf1 受容体 遺伝子 を “ノックアウト” されたマウスは通常のマウスに比べ 25% 長く生きる。また,”ROS” の害作用に対して著しい抵抗性を示す。その他の点では全く正常なマウスと差はない。
反対する意見
- コウモリとマウスは体の大きさと代謝率の点でほぼ同様であるが,コウモリは 10 倍以上も長生きする。
- グルコース飢餓酵母は確かに長生きするが,細胞の呼吸率は低下しているのではなく増加している。
なぜ代謝率が高いと老化が促進されるのか?
- 代謝率が高いと,細胞呼吸 率も高い。
- ミトコンドリアにおける電子伝達が “ROS” を生成する。
- 細胞はこれらの活性物質を無害化する酵素をもつが,これらは細胞内の以下の高分子を確実に損傷している:
- 脂質
- タンパク質
- DNA
- 損傷を受けた脂質やタンパク質は細胞内に蓄積し,とくに以下のような分裂しない細胞に蓄積しやすい:
- ニューロン
- 心筋
- リポフスチン lipofuscin と呼ばれる “加齢色素” が生成される ( リポフスチンは耳垢の主成分でもある ) 。
- カロリー制限をした動物の細胞では,リポフスチンはゆっくり蓄積する。
しかし,DNA に対する損傷が老化に伴う細胞機能の低下における重大な要素であろう。
3. 遺伝的エラーの蓄積?
これらのマウスはすべて 14 ヵ月齢である。比較的若い時に, 9 頭のマウスは致死下の放射線に暴露した。他の 9 頭は無処理の対照区である。対照区マウスは ( 左 ) は 14 ヵ月齢でも栄養状態良好で,極めて活発であるが,放射線を照射した 6 頭は死亡し,残りの 3 頭は極端な老化の兆候を示している (右) 。
支持する意見
- DNA を損傷する電離放射線を照射されたマウスは早期に老化の兆候を示す。
- 老化マウス ( あるいは老人 ) から採取した細胞は高率に突然変異や 転座 や異数性などの染色体異常を示す。
- 老人 ( ならびに 早老症 の人 ) から採取した細胞は多くの遺伝子の転写の著しい低下を示す。とくに以下に含まれる遺伝子でこの傾向が著しい:
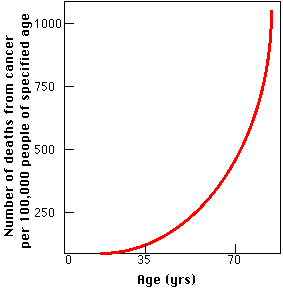
これらの変化の多くはガンを引き起こす。年齢が進むにつて,ガンの発生率が増加するが ( グラフ参照 ) ,これは偶然ではない。
早老症が示す糸口
ヒトは多くの ( 希に起こる ) 遺伝病に罹るが,早老症もその一つである。たとえば,白髪,皮膚のシワならびに短命性などが症状である。すべての例で,ゲノムの完全性を維持するのに働く,すなわち DNA 修復に働く遺伝子が突然変異遺伝子である。
- ウェルナー症候群 – 20 歳代で白髪となり,ほとんどが 40 歳代で死亡する。骨粗鬆症,白内障,アテローム性動脈硬化の様な老化の兆候を示す。 これは,DNA 修復と テロメラーゼ の維持に必要なヘリカーゼをコード化する WRN の突然変異によって起こる。
- ブルーム症候群 – 有糸分裂のエラーがないように働く他のヘリカーゼをコード化する BLM の突然変異によって起こる。この患者は高率でガンに移行する。
- 色素性乾皮症 ( XP ) – 転写に必須の遺伝子 2 個を含む DNA 修復 ( ヌクレオチド除去修復 ) に用いられるタンパク質をコード化する少なくとも 7 個のうちの 1 個の突然変異によって起こる。
- コケーン症候群 ( CS ) – DNA 修復,とくに 転写と連動したヌクレオチド除去修復 に必要な遺伝子の突然変異。この場合明瞭な老化の兆候は認められないが,短命性である。
- 毛細血管拡張性運動失調症 ( AT ) – この患者は,DNA 損傷を検出し修復の過程を開始するために必要な機能的な遺伝子 ( ATM ) 産物をもっていない。
したがって,老化は一般に多くの突然変異の結果ではなく,間違いのない以下の過程に必要なタンパク質を産生する遺伝子における突然変異の結果なのである:
- すべての遺伝子の
- 複製
- 修復
- 転写
反対する意見
なぜヒトの 70 歳がマウスの 2 歳なのか?
各事例では,細胞培養によって発育した細胞が紫外線によって照射され,その後の DNA 修復の有効性が測定された ( Hart and Setlow, 1974 ) 。
| 動物種 | 平均寿命 ( 年 ) | DNA 修復の有効性 |
| ヒト | 70 | 50 |
| ゾウ | 60 | 47 |
| ウシ | 30 | 43 |
| ハムスター | 4 | 26 |
| ラット | 3 | 13 |
| マウス | 2 | 9 |
| トガリネズミ | 1 | 8 |
老化が DNA 修復ができないための必然的な結果だとすると,ある哺乳動物が ( たとえば,マウス ) が他のもの ( たとえば,ゾウやヒト ) よりも早く老化するのはなぜか?
これはおそらくその種の外的環境 ( 補食,飢餓,寒冷 ) に対する死亡の危険度に関連すると思われる。
既に述べたように,小型の哺乳動物はほとんど老化しない。それは外的環境のために,早期に死亡するためである。これらの動物は,自身のエネルギーを速やかに費やして,
- いち早く性成熟に達する。
- いち早く自力で生存できる子どもを多数生産する。
これらの動物にとっては, DNA 修復を効率よくするために資源を費やしても自然淘汰の利点はない。突然変異が起こる前に死に至ることが多いためである。対照的に,ヒトは,
- 性成熟に達するのに長い時間を要する。
- 子供は少数で,長い期間養育しなければならない。
ヒト ( ならびに長命の哺乳動物 ) における進化の過程で,効果的な DNA 修復の方法を採用するための遺伝子が選択されてきたと考えるのはさほど不思議なことではない。
右図は種々の哺乳動物における寿命と DNA 修復の効率との関係を示す。
植物における老化
一年生ならびに越年生植物
多くの草類のような一年生植物は:
- 旺盛に発育する。
- そして,花を咲かせ,結実させる。
- その後はゆっくりとした生長が続き,以下のような生理的・形態的な変化を示す:
- 呼吸 ( 代謝 ) 速度の増大
- クロロフィルの損失
- これらの変化は老化と同等であり,植物の死につながる。
越年生植物もこれに 2 年と費やすことを除き同じパターンを示す。
このパターンは遺伝子にプログラムされたものである。養分や水を十分に補給し,日光,温度を適正に保ったとしても,植物は老化し,死ぬのである。
多年生植物
多年生植物では状況がかなり異なる。たとえば,樹木は毎年新しい維管束組織, 葉, ならびに花を形成する。年を経るにしたがい生長速度が低下するが,はっきりとした老化の兆候は見られない。病気か,風や雪の重みに対して自身の巨体を支えきれなくなり,結局死につながる。
| 最初に戻る |
January 31, 2020