| このページの内容 |
アポトーシス
すべての細胞にとって,生存の時間と死の時がある。
細胞の死には 2 つの方法がある:
- 有害な物質によって死に至る場合と,
- 自殺による場合である。
| 細胞死の電子顕微鏡写真はこちら |
損傷による死
細胞は,以下の要因によって損傷する:
- 物理的なダメージ
- 有害物質への暴露
これらのため,一連の変化が誘起される。
- 細胞(ならびに細胞小器官,たとえば ミトコンドリア)が膨化する。これは,イオンや水分の通過を制御する細胞膜の機能が破壊的損傷を受けたためである。
- 細胞の内容物が漏出する。これによって,
- 周囲の組織に炎症が起こる。
自殺による死
自殺を遂げようとする細胞は,
- 縮小する。
- ミトコンドリアが崩壊し, シトクロム C が放出される。
- 細胞表面に泡状の水疱が生じる。
- 核内のクロマチン( DNA とタンパク質 )が変性する。
- 細胞が膜で包まれた小断片に分解する。
- リン脂質 ホスファチジルセリン phosphatidylserine が露出する(通常は細胞膜内部に含まれる)。
- これには, マクロファージ や ある種の T 細胞 のような 食作用 を示す細胞に対する受容体が結合している。これらの細胞はその後,細胞断片を飲み込む。
- 食作用を示す細胞は 炎症を抑制 する サイトカイン を分泌する。
自殺による細胞死に見られる現象は整然としており,このため プログラム細胞死 programmed cell death ( PCD)と呼ばれる。プログラム細胞死の細胞機構は,たとえば 細胞分裂 のように,細胞に本来備わっているものであることが分かっている。 プログラム細胞死はアポトーシス apoptosis とも呼ばれる。 〈発音は APE oh TOE sis; 時に uh POP tuh sis 〉
なぜ細胞は自殺するのか?
1. 正常な発生過程に組み込まれている
例:
- オタマジャクシがカエルに変態する時に,尾部の吸収はアポトーシスによって起こる。
- 胎児の手や足の指の形成のとき,指の間の組織がアポトーシスによって除去される。
- 月経時の子宮内膜上皮の剥離はアポトーシスによって起こる。T
- 脳内のニューロン間に適正な シナプス 結合が形成される時,余剰の細胞はアポトーシスによって除去される。
2. 生物の生存を脅かす細胞を除去する
例:
- ウイルスに感染した細胞
- 細胞傷害性 T リンパ球 cytotoxic T lymphocytes (CTL) がウイルス感染細胞を殺す手段の 1 つにアポトーシスが関与する。[機序についてはこちら]. あるウイルスはこれに対する防衛手段を講じることがある。
- 免疫系の細胞
- 細胞性免疫反応が終わりに近づくと,体の組織への攻撃から護るために効果細胞がアポトーシスによって除去される。アポトーシスの機構がうまく働かないと, エリテマトーデス や リウマチ性関節炎 などの 自己免疫疾患 が起こる。
- DNA が損傷した細胞
- ゲノムの損傷は,細胞に対して以下のような影響がある:
- 正常な胚発生を妨げ,先天性異常の原因となる。
- ガン化する。
DNA が損傷を受けると,細胞は p53 の生合成を増加する。 p53 はアポトーシスの強力な 誘導因子 である。 p53 遺伝子の突然変異が頻繁にガン細胞に見つかっている。
- ガン細胞
- ガン治療に用いられている放射線や化学物質はある種のガン細胞にアポトーシスを引き起こす。
何が細胞に自殺を起こさせるのか?
以下の信号のバランスによる:
- ポジティブ信号( 生存し続けるために必要な信号 )の中断
- ネガティブ信号の受信
ポジティブ信号の中断
ほとんどの細胞が生存し続けるためには,他の細胞から連続的な刺激を受けとり,多くの細胞は成長している部分に付着し続ける必要がある。ポジティブ信号のいくつかの例:
- ニューロンに対する成長因子
- リンパ球 の有糸分裂に必要なインターロイキン interleukin-2 (IL-2)
ネガティブ信号の受信
- 細胞内の酸化体の量が増加する。
- これらの酸化体によって,あるいは以下のような他の要因によって DNA が損傷する。
- 紫外線
- X-線
- 化学療法薬
- 細胞表面の特異的な受容体に特定の分子が結合し,その細胞にアポトーシスと開始させる。 これらのアポトーシス活性因子には,以下のものが含まれる:
- 腫瘍壊死因子 – alpha ( TNF-a ) : これは TNF 受容体 に結合する。
- リンホトキシン lymphotoxin ( TNF-b としても知られている ) :これも TNF 受容体 に結合する。
- Fas リガンド Fas ligand ( FasL ) : Fas ( CD95 としても知られている ) と呼ばれる細胞表面受容体に結合する分子。
アポトーシスの機序
細胞の自殺,アポトーシスには 3 つの異なる機序がある。
- 細胞内に発生した信号によって起こる。
- 細胞表面の受容体にアポトーシス活性因子が結合することによる細胞外要因によって起こる。
- TNF-a
- Lymphotoxin
- Fas ligand (FasL)
- 有害な 反応性酸素分子(化合物)によって誘起される。
1. 細胞内の信号によって誘起されるアポトーシス:ミトコンドリア経路
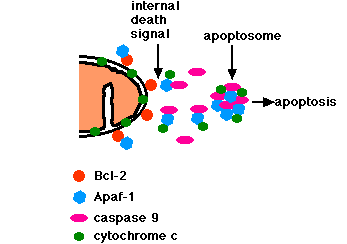
- 正常な細胞では,ミトコンドリアの外膜はタンパク質, Bcl-2 を発現する。
- Bcl-2 はタンパク質 Apaf-1 に結合する。
- 細胞内部の損傷 (たとえば, 反応性酸素分子(化合物)などの作用のため) によって, Bcl-2 は,
- Apaf-1 を放出して,
- シトクロム C がミトコンドリア外へそれ以上漏出しないように働く。
- 放出されたシトクロム c と Apaf-1 はカスパーゼ 9 caspase 9 に結合する。
- 出来上がった複合体は:
- シトクロム c
- Apaf-1
- カスパーゼ 9
- ( ならびに ATP )
はアポトソーム apoptosome と呼ばれる。
- これらは細胞質で凝集する。
- カスパーゼ 9 は 10 数種類のカスパーゼ・ファミリー( すべてタンパク質分解酵素 )の 1 つである。この酵素群はタンパク質をたいていアスパラギン酸 ( Asp ) 残基 の部位で分解するのでこの名前が付けられている。
- カスパーゼ 9 が分解する。その際,他のカスパーゼも活性化する。
- 1 種類のカスパーゼが他のものによって連続的に活性化されることによって,連続的なタンパク質分解活性が継続する。その結果:
- 細胞質内の構造タンパク質が消化され,
- 染色体 DNA が分解する。
- 細胞が食作用を受ける。
2. 細胞外の信号によって誘起されるアポトーシス:受容体経路
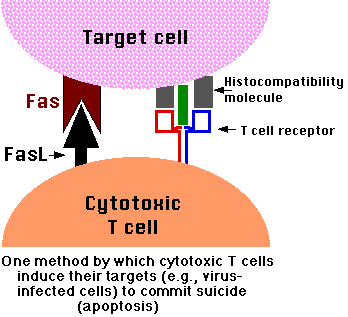
- Fas と TNF 受容体 が膜内在性タンパク質で,それらの受容体領域が細胞外に露出している。
- 相補的な アポトーシス活性因子 ( すなわち,FasL と TNF ) が結合することによって,細胞質に信号が伝わり,
- カズパーゼ 8 caspase 8 が活性化される。
- カズパーゼ 8 は ( カズパーゼ 9 と同じように ) カスパーゼ活性化を連続して開始する。これによって,
- 細胞が食作用を受ける。
例 (右): 細胞傷害性 T 細胞 が,以下の標的を認識して,結合すると,
- 細胞表面にさらに多くの FasL が生産される。
- これが,標的細胞表面の Fas を結合し,アポトーシスによる細胞死が誘起される。
アポトーシスの初期の段階は( 少なくとも線虫において )可逆的である。たいてい食細胞による食作用によって標的細胞が破壊される。
3. アポトーシス誘起因子 Apoptosis-Inducing Factor ( AIF )
ニューロンとおそらく他の細胞は,上記の 2 つの方法とは別の,カスパーゼに依存しない自滅する方法をもっている。
アポトーシス誘起因子 ( AIF ) は通常 ミトコンドリアの膜間腔 に局在するタンパク質である。 細胞が死の時であるという信号を受けとると,アポトーシス誘起因子が,
- ミトコンドリアから放出され, ( 最初の例の シトクローム C の放出の時のように )
- 核へ移動する。
- DNA に結合し,そして,
- DNA の破壊と細胞死の引き起こす。
アポトーシスと ガン
ガンの原因となるある種のウイルスは,感染した細胞のアポトーシスを妨害するために計略をはかる。
- いくつかの ヒト乳頭腫ウイルス human papilloma virus ( HPV ) は子宮頸ガンの原因となる。これらのあるものは,タンパク質 ( E6 ) を生産し,これがアポトーシスのプロモーターである p53 に結合し不活化する。
- EB ウイルス Epstein-Barr Virus ( EBV )は単球増加症と バーキット・リンパ腫の原因となる。 このウイルスは,
- Bcl-2 と同様のタンパク質を生産する。
- 細胞に自身の Bcl-2 生産を増加させる他のタンパク質を生産する。この2つの活動によって,アポトーシスに対して細胞に抵抗性をもたらす。 〈こうして,ガン細胞が増殖をし続けることを可能にしている。〉
ガン細胞はウイルスの関与がなくても,アポトーシスを避ける方策をこうじている。
- B-細胞白血病 とリンパ腫は高レベルの Bcl-2 を発現する,これによって受けるはずのアポトーシス信号を抑制している。The high levels result from a translocation of the BCL-2 遺伝子を抗体生産に関わる エンハンサー 領域に転移させて高いレベルの Bcl-2 を生産させている。 [BCL-2 についてはこちら].
- 黒色腫 ( 最も危険な皮膚ガン ) 細胞は Apaf-1 をコード化する遺伝子の発現を抑制することによってアポトーシスを回避している。
- あるガン細胞( とくに,肺ガンや大腸ガン細胞 )は FasL に結合する可溶性の “おとり” 分子を高濃度で分泌するため FasL は Fas と結合できない。そのため,細胞傷害性 T 細胞 (CTL) は 上記に示した機構 によってガン細胞を殺すことができない。
- 他のガン細胞は高濃度の FasL を発現する。細胞傷害性 T 細胞 ( CTL ) も Fas を発現するので,ガン細胞を殺そうと近づいた細胞傷害性 T 細胞 (CTL) が逆にアポトーシスを誘起されてしまう( “返り討ち”に合ってしまう )。
アポトーシスとエイズ
エイズ acquired immunodeficiency syndrome AIDS ( 後天性免疫不全症候群 ) の顕著な特徴は,患者の CD4+ T 細胞 の数が減少することである。通常,血液中に約 1,000 個/µl ある。 CD4+T 細胞は,直接あるいは間接的 ( ヘルパー細胞として ) にすべての免疫反応に対応する。それらの数が約 200 個/µl を下回ると,患者は有効な免疫反応を行うことができず,一連の危険な感染症に罹り始める。
なぜ CD4+ T 細胞が消失するのだろうか?
ヒト免疫不全ウイルス HIV (human immunodeficiency virus) は CD4+ T 細胞に感染する。しかしこれが,主因ではない。確かに HIV に感染した CD4+ T 細胞が患者の血中に見られるが,その数は 1/100,000 以下である。
それでは,感染していない CD4+ T 細胞がなぜそうもたくさん死んでしまうのか?
答えは明瞭,アポトーシスである。
その機構はまだ解明されていないが,いくつかの可能性がある。その 1 つを紹介する。
- すべての T 細胞は,感染したものもしていないものも Fas を発現する。
- HIV 感染細胞における HIV 遺伝子 ( Nef と呼ばれる ) の発現によって,
- 細胞が高濃度の FasL を細胞表面に発現する。
- ただし,自身の Fas との相互作用による自己破壊は回避されている。
- しかし,感染した T 細胞が感染していない T 細胞に遭遇すると ( たとえば,リンパ節内で ),感染していない細胞上の Fas と FasL が相互作用して,アポトーシスが起こってしまう。
アポトーシスと 臓器移植
- 前眼房
- 精巣
が, “免疫学的寛容部位” であることが示されている。 これらの器官内の抗原が免疫反応を誘起しないのである。
これらの部位の細胞は,他の部位の細胞と異なり,常に高いレベルの FasL を発現していることが分かっている。したがって,抗原に反応する T 細胞( これは Fas を発現している )がこれらの部位に入ると逆に細胞死を誘起されてしまう。
この知見は移植臓器の拒絶反応を抑制する新しい方法となる可能性を示唆する。
移植された腎臓,肝臓,心臓などの,少なくとも一部の細胞で高いレベルの FasL を発現させることができれば,宿主の細胞媒介性の免疫システムの T 細胞による攻撃から移植臓器を護ることになる。それができれば,現在移植患者に対してその生存の間行われている免疫抑制剤での処理を軽減できるか,全く必要がなくなることになる。
現在のところ,実験動物における結果も含め検討されている。 FasL を発現させるようにした 同種移植 によって,腎臓では成功率が上がったが,心臓またはランゲルハンス島ではうまくいっていない。
| 最初に戻る |
| メニューのページへ戻る |
February 03, 2020